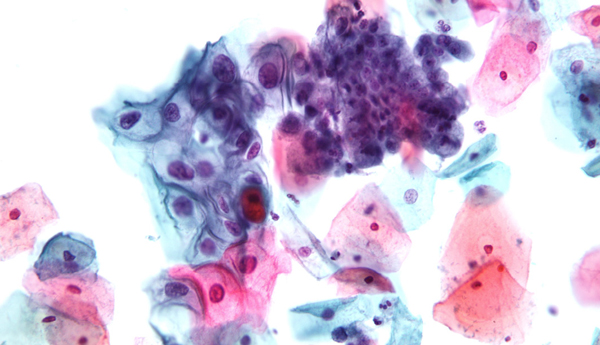
Het nieuwe HPV-bevolkingsonderzoek voldoet niet
8 reactiesOPINIE
Kans op overdiagnostiek en overbehandeling stijgt
In 2016 schakelt Nederland over op de screening op baarmoederhalskanker via een virustest. De specificiteit en sensitiviteit daarvan zijn echter onvoldoende en dat zal veel onnodige ongerustheid en zorgconsumptie tot gevolg hebben, waarschuwen pathologen Giard en Riemersma.
We staan in ons land aan de vooravond van de overgang naar een nieuwe opzet en uitvoering van het bevolkingsonderzoek (BVO) baarmoederhalskanker: van een primair cytologisch onderzoek van het bekende ‘uitstrijkje’, in sommige gevallen uitgebreid met HPV-onderzoek, naar primaire HPV-screening van het uitstrijkmateriaal van vrouwen tussen de 30 en 60 jaar. De voorgenomen overgang is gebaseerd op een advies van de Gezondheidsraad uit 2011.
Het huidige Nederlandse BVO staat wereldwijd als zeer goed bekend. In de afgelopen tien jaar zijn vrijwel alle laboratoria overgegaan op de zogenaamde dunnelaagmethode, wat resulteerde in een daling van het aantal niet beoordeelbare uitstrijken ten opzichte van de klassieke uitstrijk op een glaasje. Tot 2007 werden de uitstrijkjes uitsluitend beoordeeld door middel van cytologie. Daarna werd bij uitstrijkjes met geringe cytologische afwijkingen een aanvullende test gedaan om de aanwezigheid van high-risk HPV (hr-HPV) in de cellen aan te tonen dan wel uit te sluiten. De gedachte hierbij is dat als er geen hr-HPV aanwezig is, minder stringente follow-up noodzakelijk is. Of deze veranderingen effectief zijn geweest, is in Nederland tot op heden niet systematisch onderzocht. Toch werd door de minister van VWS op basis van het genoemde Gezondheidsraad-advies in 2012 besloten het bevolkingsonderzoek radicaal te veranderen.
Ernstige twijfels
Binnen de beroepsgroep van pathologen bestaan ernstige twijfels of het een verstandig besluit was en is om het BVO op deze manier te veranderen. De cervixcytologie scoort zeker geen 100 procent sensitiviteit en specificiteit; dat doet overigens geen enkel diagnosticum. Om een optimaal resultaat te kunnen behalen bij een BVO is de opkomst van groot belang. Hier ligt een kernprobleem; bij 60 procent van de vastgestelde cervixcarcinomen werd er geen voorafgaand uitstrijkje gemaakt. Vrouwen met een verhoogd risico nemen dus vaak niet deel.
Ziektedetectie is niet het primaire doel van kankerscreening maar het middel om de incidentie van kanker en het lijden en sterven aan de betreffende tumor binnen de onderzochte populatie te verminderen, dit afgewogen tegen een vooraf gestelde maximale prijs per gewonnen levensjaar. Als echter het ontdekken van (pre)maligne aandoeningen door middel van screening vooropstaat, bestaat het gevaar van overdiagnostiek en overbehandeling. Niet de sensitiviteit (de detectiekans van ziekte), maar de vals-alarmkans (=100%-specificiteit) is de bepalende factor voor de geschiktheid van een test voor kankerscreening, want die geeft de kans op overdiagnostiek- en behandeling aan.
Vanuit dit perspectief doet zich de vraag voor welke testmethode nu het beste gebruikt kan worden bij dit bevolkingsonderzoek. Om een rationele keuze te kunnen maken tussen screeningstesten moeten twee vragen worden beantwoord:
1 Welke van de testmethoden blijkt bij vergelijkend onderzoek – binnen het pakket van eisen waaraan een screeningstest moet voldoen – het beste te functioneren? Hierbij gaat het niet alleen om de succeskans om ziekte te detecteren maar vooral ook om de kans op overdiagnostiek en overbehandeling.
2 Blijkt de toepassing van de op grond van betere testeigenschappen gekozen alternatieve methode ook te resulteren in een betere realisering van de screeningsdoelstellingen? Deze vraag is pas te beantwoorden na jarenlang trialonderzoek.
Sterk verschillend
Bij vraag 1, de vergelijking van cytologisch onderzoek versus primaire hr-HPV-diagnostiek, is het allereerst van belang dat men zich realiseert dat het hier om twee essentieel verschillende soorten testen gaat. Cytologie bepaalt de aan- of afwezigheid van ziekte, een hr-HPV-test duidt slechts een risicofactor aan. De interpretatie van uitkomsten is daardoor ook sterk verschillend, wat gevolgen heeft voor het beoordelen van de testeigenschappen, met name de gevoeligheid (sensitiviteit) en de vals-alarmkans (specificiteit). Omdat met de hr-HPV-test virusinfecties worden aangetoond die later weer zullen uitdoven, is de kans op overdiagnostiek al op voorhand groter dan bij cytologisch onderzoek. De gevoeligheid van de hr-HPV-test zou daarentegen in theorie groter kunnen zijn.
Wie naar een betrouwbaar wetenschappelijk gefundeerd antwoord zoekt, komt terecht in een tsunami van circa 140 duizend artikelen over de etiologische betekenis van HPV, HPV-testen, verge-lijkend onderzoek HPV-diagnostiek versus cytologie (soms met HPV-triage) en implementatietrials. Vergelijkend onderzoek over langetermijneffecten qua baarmoederhalskankersterfte bij primaire HPV-screening versus cytologie ontbreekt vooralsnog. Welke conclusies zijn er op dit moment wel te trekken?
Over de accuratesse van HPV-testen is ook veel gepubliceerd, maar lang niet alle studies voldoen aan methodologische vereisten; een onafhankelijke beoordelingsstandaard ontbreekt vaak, waardoor een verificatiebias ontstaat, alleen positieve hr-HPV-testuitslagen leiden tot vervolgdiagnostiek, niet de negatieve.1
Vals alarm
Een recente meta-analyse laat slechts twaalf artikelen zien die voldeden aan de inclusiecriteria. De onderzoekers stelden vast dat de sensitiviteit van de hr-HPV-test varieerde tussen 58 en 94 procent en de specificiteit tussen 2 en 95 procent. De gepoolde sensitiviteit bedroeg 83 procent en de gepoolde specificiteit 71 procent.2 De verwachte lagere specificiteit van de hr-HPV-test werd in diverse onderzoeken, waaronder een Cochrane-evaluatie, bevestigd.3
Ter vergelijking, in het Gezondheidsraad-advies van 2011 is voor de kosteneffectiviteitsstudie gerekend met een sensitiviteit van de hr-HPV-test van 92 procent en een specificiteit van 96 procent!
Juist omdat deze vals-alarmkans bij kankerscreening zo doorslaggevend is, is de hr-HPV-test zeker niet superieur aan cytologie. Primaire screening op hr-HPV zal dus leiden tot meer onnodige diagnostiek c.q. behandeling en onnodige ongerustheid bij vrouwen.
Er zijn eveneens zeer veel publicaties verschenen die een vergelijking maken tussen cytologie en hr-HPV voor de detectiekans op (pre)maligne afwijkingen. Pileggi e.a. vonden slechts acht studies die aan de eisen voldeden en bij hun conclusies waren ze zeer terughoudend.4 Met name de lagere specificiteit van de hr-HPV-test tegenover de cytologie baarde zorgen. Een enkele maanden geleden gepubliceerde grote Amerikaanse studie laat zelfs ook een lagere sensitiviteit zien van de hr-HPV ten opzichte van cytologie voor de detectie van cervixcarcinomen.5 Die lagere sensitiviteit van hr-HPV-test werd zeer recentelijk bevestigd in een Belgische studie met 1 miljoen uitstrijken en follow-updata.6
Wat betreft de tweede vraag, de winst- en verliesrekening voor de deelnemende vrouwen, is een veel bredere en langdurige evaluatie nodig. Hierbij zijn niet alleen de diagnostische kenmerken van de screeningstest relevant, maar ook de effecten op morbiditeit en mortaliteit van de deelnemers en schatting van het number needed to screen. Deze studies zijn momenteel echter niet voorhanden.
Foutieve aannames
De hr-HPV-test is zeker nieuw in vergelijking tot de decenniaoude cytologie, maar niet zodanig overtuigend superieur dat dit een radicale verandering van het bevolkingsonderzoek rechtvaardigt. Zeker in het licht van de uitkomsten van recente meta-analyses zijn de aannames van de Gezondheidsraad in het rapport van 2011 foutief en de daarop gebaseerde conclusies zijn gezien het hierboven geschrevene niet overtuigend.
Er lijkt eerder te zijn toegewerkt naar een keuze op grond van hooggespannen verwachtingen in plaats van op basis van solide wetenschappelijke argumenten.
auteur
prof. dr. Raimond Giard
klinisch patholoog, klinisch epidemioloog en jurist
dr. Sietske Riemersma
klinisch patholoog
contact
s.riemersma@labpon.nl; cc: redactie@medischcontact.nl
Gemelde belangenverstrengeling: Riemersma: speakers fees: Lilly, Amgen; travel grant: Roche; advisory board: Pfizer, Amgen; research support: Amgen, Novartis. Giard: geen.
Commentaar NVOG
Giard e.a. hebben bij elke verandering in het bevolkings-onderzoek baarmoederhalskanker (in 1996, 2007 en nu) bezwaar gemaakt, met name tegen invoering van HPV-testen. Hoewel zij erkennen dat het huidige uitstrijkje ‘zeker geen honderd procent’ scoort, verdoezelen zij dat cytologie met zo’n 60 procent sensitiviteit voor significante laesies niet voldoet voor het opsporen van behandelbare voorstadia en dat daardoor de bijdrage van het huidige bevolkingsonderzoek aan het reduceren van sterfte door baarmoederhalskanker helaas zeer beperkt is. Giard en Riemersma gaan aan dit manco van het uitstrijkje voorbij, terwijl ze wel het verwijt maken dat sterftereductie nog niet is uitgezocht voor HPV-testen. Inderdaad laten die resultaten nog enkele decennia op zich wachten, maar intussen weten we wel dat met HPV-testen meer behandelbare voorstadia van kanker worden opgespoord dan met cytologie.
Zij ontkennen aan de hand van een niet-gerandomiseerde studie het in grote binnen- én buitenlandse gerandomiseerde studies aangetoonde voordeel van screening met HPV-testen. Ze leggen daarbij nadruk op de ‘vals-alarm’-kans, zonder kritiek te uiten op de huidige onverantwoorde kans op een fout-negatieve uitkomst bij de beoordeling van een uitstrijkje. In het nieuwe bevolkingsonderzoek wordt overigens rekening gehouden met vaker verwijzing naar de gynaecoloog, die terughoudend zal zijn met behandelen.
De Gezondheidsraad heeft in 2011 op basis van Nederlandse en buitenlandse studies besloten tot verbetering van het bevolkingsonderzoek op baarmoederhalskanker door HPV-testen in te voeren als primair screeningsinstrument. Hierbij worden overigens alle HPV-positieve gevallen nog eens extra – maar nu dus selectief en dus potentieel beter – bekeken met het conventionele uitstrijkje. Deze allang noodzakelijke verbetering van het bevolkingsonderzoek moet niet worden tegengehouden door bijna vijf jaar na beslissing daartoe een discussie te beginnen met ondeugdelijke argumenten.
prof. dr. René Verheijen
gynaecologisch oncoloog, Utrecht, lid van de RIVM programmacommissie Bevolkingsonderzoek Baarmoederhalskanker, lid van het bestuur van de NVOG Werkgroep Cervix Uteri
dr. Ruud Bekkers
gynaecologisch oncoloog, Nijmegen, voorzitter van de NVOG Werkgroep Cervix Uteri
voetnoten
1. Xue X, Kim MY, Castle PE, Strickler HD. A new method to address verification bias in studies of clinical screening tests: Cervical cancer screening assays as an example. J Clin Epidemiol [Internet]. Elsevier Inc; 2014; 67 (3): 343-53. Available from: http://dx.doi.org/10.1016/j.jclinepi.2013.09.013.
2. Yin D, Jiang Y, Wang N, Ouyang L, Lu Y, Zhang Y, et al. The diagnostic value of serum hybrid capture 2 (CH2) HPV DNA in cervical cancer: a systematic review and meta-analysis. Tumor Biol [Internet]. 2014; 35 (9): 9247-53. Available from: http://link.springer.com/10.1007/s13277-014-2214-4.
3. Arbyn M, Roelens J, Simoens C, Buntinx F, Paraskevaidis E, Ppl M, et al. Human papillomavirus testing versus repeat cytology for triage of minor cytological cervical lesions ( Review ) Human papillomavirus testing versus repeat cytology for triage of minor cytological cervical lesions. Cochrane Libr. 2013; (3): 1-200.
4. Pileggi C, Flotta D, Bianco A, Nobile CG a, Pavia M. Is HPV DNA testing specificity comparable to that of cytological testing in primary cervical cancer screening? Results of a meta-analysis of randomized controlled trials. Int J Cancer 2014; 135 (1): 166-77.
5. Blatt AJ, Kennedy R, Luff RD, Austin RM, Rabin DS. Comparison of cervical cancer screening results among 256,648 women in multiple clinical practices. Cancer Cytopathol [Internet]. 2015; (May): n/a – n/a. Available from: http://doi.wiley.com/10.1002/cncy.21544
6. Benoy I, Depuydt C, Sahebali S, VandenBroeck D, Jonckheere J, Salembier G, Vereecken A, Bogers J. Screening advantage of cytovirological co-testing tot prevent invasive cervical cancer: The AML experience. Abstract HPV15-0164 presented at the 30th IPV conference, Lisbon 17-21 sept 2015.