Ziekenhuizen zuinig met dure darmkankerbehandeling
Ongewenste variatie in de behandeling van uitgezaaide dikkedarmkanker
2 reacties
Uit een onderzoek in twintig ziekenhuizen blijkt dat lang niet alle patiënten met uitgezaaide dikkedarmkanker naast een behandeling met chemotherapie ook doelgerichte therapie, zoals bevacizumab krijgen, wat de richtlijn aanbeveelt. Financiële argumenten lijken hierbij een rol te spelen.
De laatste decennia is de prognose van patiënten met uitgezaaide dikkedarmkanker verbeterd, onder andere door nieuwe geneesmiddelen, zoals bevacizumab en een anti-EGFR-antilichaam. De huidige standaardbehandeling voor deze patiënten is: systemische therapie bestaande uit chemotherapie (fluoropyrimidines, oxaliplatine en/of irinotecan) en doelgerichte therapie: bevacizumab (antilichaam tegen de vasculaire endotheliale groeifactor, VEGF), en cetuximab of panitumumab (antilichamen tegen de epidermale groeifactorreceptor, EGFR).1 Deze doelgerichte therapie is echter kostbaar en wordt niet bij alle patiënten aan de standaardtherapie toegevoegd.
Er blijken enorme verschillen in het voorschrijfgedrag
Voor de behandeling met doelgerichte therapie bestaan weinig contra-indicaties. Voor bevacizumab zijn geen predictieve factoren bekend. Voor de anti-EGFR-therapie is de indicatie in de loop der jaren gewijzigd. Kregen aanvankelijk patiënten met een KRAS wildtype tumor deze behandeling, tegenwoordig komen alleen patiënten met een linkszijdige primaire én die met een KRAS/NRAS/BRAFV600E wildtype tumor voor deze behandeling in aanmerking. Hiertoe dient voorafgaand aan de systemische behandeling de mutatiestatus van de tumor te worden bepaald. Bevacizumab wordt doorgaans als onderdeel van een eerstelijnsbehandeling in combinatie met chemotherapie toegediend, en in dat geval wordt anti-EGFR-therapie als monotherapie of in combinatie met chemotherapie toegediend vanaf de tweede lijn. Het gebruik van deze geneesmiddelen heeft in klinische studies tot een zodanige verbetering van de prognose geleid dat deze middelen zijn opgenomen in de landelijke richtlijn.
Voorschrijfgedrag
Recentelijk hebben het Amsterdam UMC, het UMC Utrecht en het Integraal Kankercentrum Nederland (IKNL) het voorschrijfgedrag van oncologische geneesmiddelen bij patiënten met uitgezaaide dikkedarmkanker onderzocht. Het ging om geneesmiddelen die volgens de richtlijn tot de standaardbehandeling behoren. Het onderzoek is gedaan in twintig willekeurig gekozen Nederlandse ziekenhuizen in de periode 2008 tot 2015.2
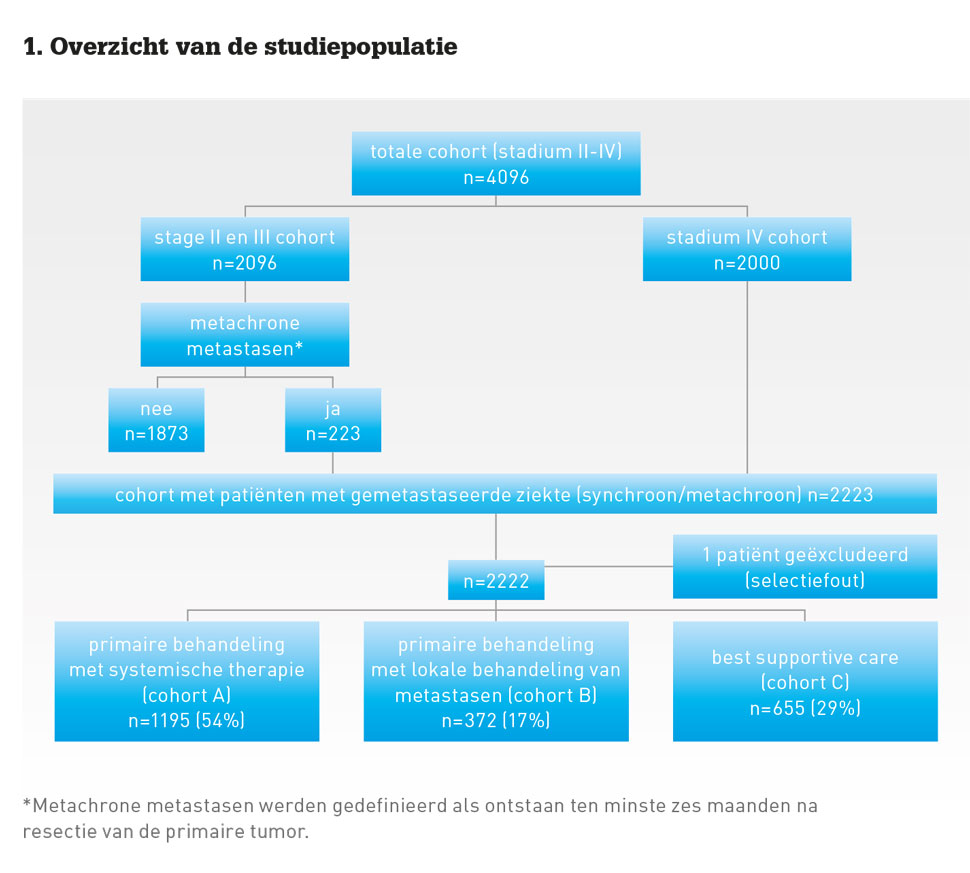
Er werden ruim tweeduizend patiëntendossiers uit vier academische, acht STZ-ziekenhuizen (Samenwerkende Topklinische opleidingsZiekenhuizen) en acht perifere ziekenhuizen geëvalueerd. Patiënten werden ingedeeld in drie cohorten. Cohort A bestond uit patiënten die in eerste instantie systemische therapie kregen (dus chemotherapie in combinatie met een doelgerichte therapie: bevacizumab, c.q. anti-EGFR-therapie). Cohort B waren patiënten die in eerste instantie werden behandeld met lokale behandeling van metastasen en pas systemische therapie ontvingen bij een recidief. Cohort C, ten slotte, betrof patiënten die uitsluitend best supportive care ontvingen (zie figuur 1). In totaal werden 1307 patiënten (59%) behandeld met systemische therapie gedurende hun ziektetraject (de patiënten uit cohort A en een deel van de patiënten uit cohort B). De meest gebruikte behandelregimes voor patiënten die uitsluitend met systemische therapie werden behandeld (en dus geen lokale behandeling van metastasen ondergingen) bestonden uit capox-B (capecitabine, oxaliplatine en bevacizumab; 37%), capox (24%) en capecitabine monotherapie (20%).
Mutatiestatus
Van de 1307 patiënten die in aanmerking kwamen voor de doelgerichte therapie hebben in totaal 796 patiënten (61%) deze als onderdeel van hun systemische behandeling gekregen. Dit betrof bij het merendeel van hen (55% van 1307) bevacizumab. Bij slechts 47 procent van alle patiënten die systemische therapie ontvingen werd de (K)RAS mutatiestatus van hun tumor bepaald, en slechts een minderheid van de patiënten met een (K)RAS wildtype tumor (45% van 301 patiënten) ontving anti-EGFR-therapie. Er is dus sprake van onderbehandeling, want deze percentages zijn veel lager dan op grond van eventuele contra-indicaties te verwachten is.
Patiënten zijn niet op de hoogte van individueel ziekenhuisbeleid
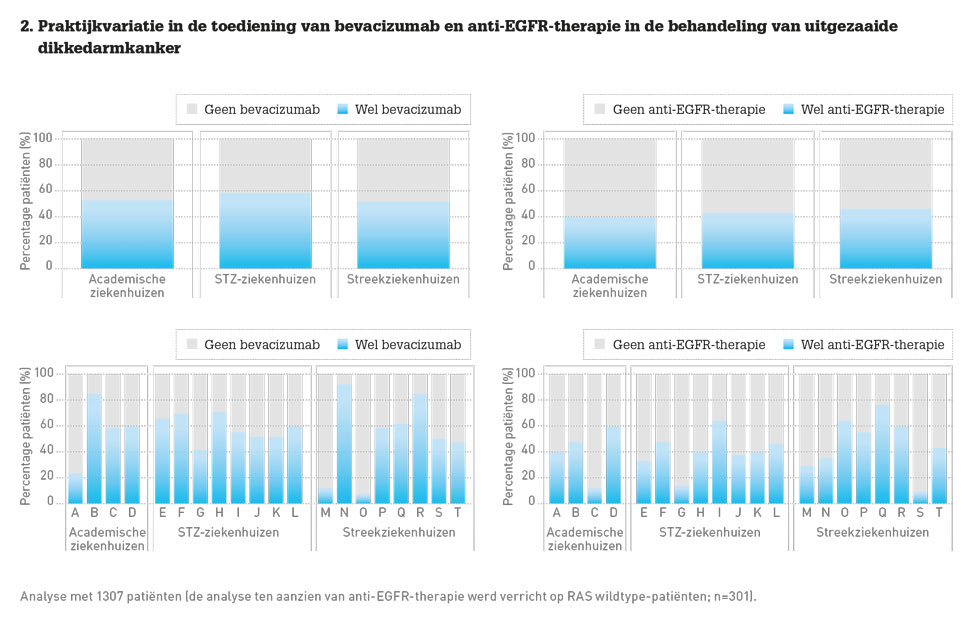
Er was geen verschil in voorschrijfgedrag tussen verschillende typen ziekenhuis (academisch, STZ, perifeer). Er waren echter enorme verschillen in dit voorschrijfgedrag tussen individuele ziekenhuizen. Het percentage patiënten dat doelgerichte therapie kreeg, varieerde tussen individuele ziekenhuizen van 8 tot 92 procent voor bevacizumab en van 10 tot 75 procent voor anti-EGFR-therapie (zie figuur 2). Er was weliswaar een omgekeerde correlatie tussen het voorschrijven van de medicijnen en een hogere leeftijd en meer comorbiditeit bij patiënten (zoals hypertensie, een cardiovasculaire voorgeschiedenis, trombose en nierziekten), maar tussen de individuele ziekenhuizen bleken deze patiëntkarakteristieken niet verschillend en derhalve niet verklarend voor de variatie tussen individuele ziekenhuizen. Figuur 2 toont de enorme verschillen tussen deelnemende ziekenhuizen in het behandelen met bevacizumab en met anti-EGFR-therapie. Daarnaast werd een aanzienlijk deel van de patiënten zonder comorbiditeit niet behandeld met doelgerichte therapie (bevacizumab: 15%, anti-EGFR-therapie: 20%), hetgeen duidelijk maakt dat comorbiditeit niet de enige reden was om af te wijken van de richtlijn. In cohort A hadden patiënten die werden behandeld met doelgerichte therapie een overlevingsvoordeel ten opzichte van patiënten die niet met deze middelen werden behandeld, conform de resultaten van eerdere studies. Dit overlevingsvoordeel hield stand na correctie voor eventueel verstorende variabelen.
Afweging
Concluderend kreeg in strijd met de richtlijn dus slechts een minderheid van de patiënten die hiervoor in aanmerking komen een behandeling met bevacizumab of anti-EGFR-therapie.
Vanzelfsprekend is enige variatie in voorschrijfgedrag tussen verschillende ziekenhuizen en tussen verschillende behandelaren te verwachten. Dit ontstaat door een afweging te maken in de behandeling voor elke individuele patiënt op basis van onder andere comorbiditeit, eventuele contra-indicaties voor geneesmiddelen, en de wens van de patiënt. Dit wordt ook wel zogenaamde ‘gewenste praktijkvariatie’ genoemd. De variatie die wij in deze studie vonden laat echter zien dat er voornamelijk praktijkvariatie bestaat ten aanzien van het voorschrijven van dure geneesmiddelen. Deze variatie lijkt niet te worden bepaald door de eerder genoemde individuele patiëntkenmerken of aanbevelingen zoals beschreven in de landelijke richtlijn, maar door individueel ziekenhuisbeleid. Dit kan als ongewenst worden beschouwd, met mogelijke gevolgen voor de overleving en kwaliteit van leven van de individuele patiënt.
Financiële factoren
We hebben aanzienlijke verschillen vastgesteld in het voorschrijfgedrag tussen individuele ziekenhuizen van met name dure geneesmiddelen in de behandeling van uitgezaaide dikkedarmkanker, die niet volledig zijn te herleiden tot patiënt-gerelateerde factoren. Dit kan leiden tot een onnodig slechtere uitkomst van behandeling bij patiënten. Dit onderzoek geeft geen inzicht in de redenen voor deze ongewenste praktijkvariatie, maar zeer waarschijnlijk spelen financiële factoren hierbij een rol. Patiënten zijn niet op de hoogte van individueel ziekenhuisbeleid, omdat dergelijke strategieën niet publiekelijk bekend worden gemaakt. De doelgerichte geneesmiddelen zijn duur, met gedurende het patent gemiddelde kosten van 25.000 euro per patiënt. In Nederland krijgen ongeveer 14 duizend mensen per jaar dikkedarmkanker, en bij ongeveer de helft van hen ontstaan uitzaaiingen. Bij het merendeel van patiënten met uitzaaiingen is er een indicatie voor systemische therapie.
Goede monitoring
De uitkomsten van dit onderzoek onderstrepen het belang van goede monitoring van de behandeling van oncologische patiënten in de dagelijkse praktijk. Initiatieven zoals het Prospectief Landelijk Colorectaal Carcinoom Cohort (plcrc.nl) kunnen hier in hoge mate aan bijdragen.3 Het PLCRC biedt een infrastructuur voor het verzamelen van klinische gegevens, patiëntgerapporteerde uitkomsten en het opslaan van bloed en tumorweefsel van patiënten met dikkedarmkanker. Dit gebeurt na het verkrijgen van toestemming van de patiënt. Er kunnen valide medische redenen zijn om bij individuele patiënten af te wijken van richtlijnaanbevelingen, maar deze dienen dan in het medisch dossier te worden gedocumenteerd. Als deze afwijkingen zijn gebaseerd op een algemeen beleid van een ziekenhuis moeten ook patiënten hierover worden geïnformeerd.
auteurs
Lotte Keikes, internist in opleiding, Amsterdam UMC locatie AMC
prof. dr. Kees Punt, medisch oncoloog, Julius Centrum, UMC Utrecht
contact
c.j.a.punt@umcutrecht.nl
cc: redactie@medischcontact.nl
Lees meerVoetnoten
1. Richtlijnen Oncologische Zorg. Colorectaal carcinoom. Integraal Kankercentrum Nederland (IKNL) 2014.
2. Keikes L, Koopman M, Stuiver MM, Lemmens V, van Oijen MGH, Punt CJA. Practice variation on hospital level in the systemic treatment of metastatic colorectal cancer in The Netherlands: a population-based study. Acta Oncol. 2020; 59: 395-40
3. Boerbach JP, Kurk SA, Coebergh van den Braak RR, Dik VK, May AM, Meijer GA, Punt CJ, Vink GR, Los M, Hoogerbrugge N, Huijgens PC, Ijzermans JN, Kuipers EJ, de Noo ME, Pennings JP, van der Velden AM, Verhoef C, Siersema PD, van Oijen MG, Verkooijen HM, Koopman M. Prospective Dutch colorectal cancer cohort: an infrastructure for long-term observational, prognostic, predictive and (randomized) intervention research. Acta Oncol. 2016;55:1273-80
download dit artikel (pdf)















Fred Bekker
psychiater, Apeldoorn
Schokkend. Ik dacht dat het in strijd met een richtlijn behandelen vooral een probleem is dat in mijn eigen vak plaats vindt. Daarin spelen financiële aspecten echter geen vergelijkbare rol. Ik ken mijn vakgenoten en andere medisch specialisten echte...r doorgaans als integere bevlogen vakmensen. Het is toch niet voorstelbaar dat die zich laten bepalen door dit soort financiële zaken. Welke andere factoren zouden hier nog meer mee kunnen spelen?
Natasha
basisarts
Marktwerking,waar het beschikbaar zijn van een psychiater voor je kind afhangt de gemeente waarin je woont, en de kwaliteit van de chemotherapie van je oma afhangt van het ziekenhuis dat ze uitkiest.