Een tomtom voor de chirurg
Plaats een reactieTECHNIEK
Intra-operatieve navigatie voor opsporing van laesies
Met nieuwe technieken kunnen operateurs tijdens de operatie haarscherp navigeren. Dat verbetert het operatieresultaat en verhoogt de patiëntveiligheid. Vier onderzoekers leggen uit hoe. Zij zijn bezig met de validatie en implementatie van deze technieken en wonnen daarmee de Innovation for Health Award 2014.
Intra-operatieve lokalisatie van laesies gebeurt sinds jaar en dag aan de hand van anatomische herkenningspunten en de anatomische kennis van de snijdend specialist.1 De laatste jaren is het door middel van preoperatieve beeldvorming mogelijk geworden om laesies in 3D te identificeren. Maar daardoor is het voor de specialist wel steeds moeilijker geworden om deze veelal complexe datasets in gedachten te combineren met wat hij of zij ziet en voelt tijdens de ingreep.
Net als in het verkeer kunnen navigatietechnieken, gebruikmakend van virtuele datasets, de specialist helpen om deze toegenomen complexiteit het hoofd te bieden.2 Dit kan bij verschillende interventies van toegevoegde waarde zijn. Bijvoorbeeld bij gerichte biopsieën, lokale ablaties en de chirurgische verwijdering van laesies. Zelf verwachten we dat de meerwaarde het grootst zal zijn tijdens complexere interventies die gericht zijn op de identificatie van kleine laesies. Zo kan bij een klinische indicatie waar
laesies – bijvoorbeeld tumor(en) – goed in 3D geïdentificeerd kunnen worden met behulp van preoperatieve beeldvorming, intra-operatieve navigatie in deze beelden de specialist helpen om chirurgische instrumenten direct naar deze laesies toe te leiden, wat de nauwkeurigheid ten goede zou komen.
Nucleaire beeldvorming
Doordat de hedendaagse nucleaire beeldvormingstechnieken van oncologische ziektebeelden vergevorderd zijn, vormen deze in onze ogen een belangrijk uitgangspunt voor het gebruik van navigatietechnieken: de virtuele landkaart als het ware. Binnen de nucleaire geneeskunde wordt gebruikgemaakt van radioactieve tracers die zich kunnen binden aan specifieke moleculaire markers. Om deze radioactieve tracers in ‘beeld’ te brengen bestaan er twee vormen van 3-D beeldvorming die in aanmerking komen voor intra-operatieve navigatie, namelijk: single photon emitted computed tomography (SPECT) en positron emitted tomography (PET). Door de nucleaire beeldvorming te combineren met CT of MRI, wordt de accumulatie van de radioactieve tracer binnen de anatomische context van de patiënt geplaatst, waarbij deze gecombineerde datasets als uitgangspunt voor navigatiegestuurde interventies en operaties kunnen dienen.3 4
Tracking
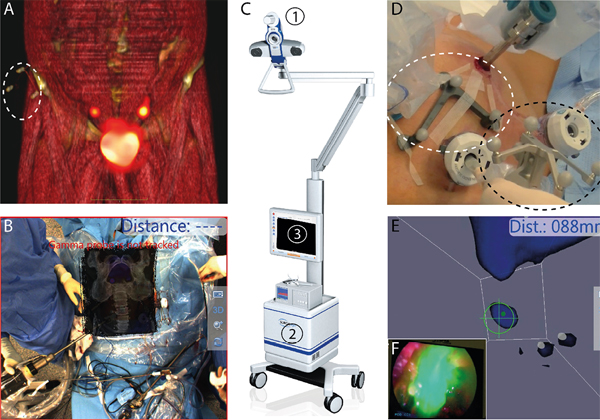
Waar een programma als Google Maps gebruikmaakt van gps-coördinaten, zijn voor navigatie in patiëntenbeelden zogenaamde trackers nodig die het mogelijk maken om de verkregen preoperatieve beelden te linken aan de positie van de patiënt (zie figuur 1A op blz. 284: de tracker is omcirkeld). Via deze tracker kunnen de beelden in de operatiekamer op de patiënt teruggeprojecteerd worden
(zie figuur 1B) en kunnen de chirurgische instrumenten in deze virtuele kaart genavigeerd worden.
Over het algemeen past men twee verschillende tracking-technieken toe: optische tracking en elektromagnetische tracking. Optische tracking maakt gebruik van lichtreflecterende trackers op de patiënt en op het chirurgische instrument (zie figuur 1D). Doordat deze trackers een specifiek (infrarood) lichtsignaal, uitgezonden door het navigatiesysteem, weerkaatsen, wordt het mogelijk om te bepalen waar de patiënt (en dus de virtuele kaart) zich bevindt ten opzichte van het genavigeerde chirurgische instrument (zie figuur 1E). Elektromagnetische tracking werkt eigenlijk hetzelfde, maar maakt gebruik van een magnetisch veld en elektromagnetische spoelen op de trackers in plaats van de reflectie van licht. Een voordeel van beide technieken is dat de trackers makkelijk en steriel geplaatst kunnen worden op het lichaam van de patiënt en dat dit op meerdere plekken kan. Dit is meteen ook een groot nadeel van beide technieken: doordat ze geplaatst worden op niet-rigide structuren is beweging van de laesies ten opzichte van de patiënten-tracker mogelijk. Vooral bij zachte weefsels en beweeglijke organen kan dit tot forse afwijkingen leiden.

Schildwachtklierprocedure
Binnen verschillende oncologisch gerichte studies zijn wij bezig met de validatie en implementatie van navigatietechnieken die gebaseerd zijn op preoperatieve (nucleaire) beeldvorming. Daarmee hebben wij de Innovation for Health Award 2014 gewonnen. De schildwachtklierprocedure vormt hier een goed uitgangspunt. Dit omdat deze radiogeleide procedure een breed draagvlak heeft en well-established is in de kliniek, maar dat er desondanks nog verbetering mogelijk is. Verder gaan we ervan uit dat als we de navigatietechnieken geoptimaliseerd hebben voor de verschillende anatomische locaties die we tegenkomen bij de schildwachtklierprocedure, deze met relatief weinig aanpassingen ook geschikt gemaakt kunnen worden voor andere toepassingen.
Binnen de urologie hebben we voor de schildwachtklierprocedure bij penis- en prostaatkanker laten zien dat we zowel een gammaprobe als een fluorescentie-laparoscoop optisch konden navigeren naar schildwachtklieren die een hybride contrastmiddel bevatten dat zowel radioactief als fluorescent is (indocyanine groen-99mTc-nanocolloid).5 6 Voor oppervlakkig gelegen klieren in de lies hebben we laten zien dat de afwijking in de accuraatheid van preoperatieve SPECT-CT-gebaseerde navigatie rond de 5 mm ligt.5 Voor diepere iliacale klieren kan deze afwijking echter oplopen tot centimeters.
Een manier om te controleren of de navigatie accuraat is, en eventueel te compenseren voor een opgetreden afwijking – bijvoorbeeld omdat de positionering van de patiënt op de operatietafel anders is dan wanneer de preoperatieve beelden vervaardigd worden – is toepassing van een intra-operatieve detectietechniek die deze afwijking kan opvangen.6 Zo kunnen de gammastralen van indocyanine groen-(ICG)99mTc-nanocolloid tijdens de ingreep gedetecteerd worden met een gammaprobe, terwijl een nabij-infrarode fluorescentiecamera de schildwachtklier kan helpen visualiseren als het genavigeerde instrument deze op minder dan één centimeter genaderd is. We hebben met deze benadering laten zien dat met afnemende virtuele afstand een toenemend fluorescentiesignaal werd gezien (zie figuur 1F). Met andere woorden, gebruik van real-time fluorescentie-verificatie tijdens het navigatieproces kan navigatiefouten die binnen deze één-centimetermarge vallen, helpen corrigeren.6
Uitdagingen
Ons doel is om de techniek verder te optimaliseren voor chirurgische ingrepen in complexe anatomische regio’s waar inschatting van locatie en diepte van de laesie vaak lastig is, bijvoorbeeld het hoofd-halsgebied en het kleine bekken. Ook onderzoeken we het gebruik van navigatie in de diagnostische setting.7 Daarbij valt bijvoorbeeld te denken aan biopsieën, waarbij heel specifiek een biopt kan worden genomen van een verdachte plek die geïdentificeerd is met behulp van eerdere beeldvorming.
Een van de grootste uitdagingen die naar voren komt tijdens het gebruik van verschillende modaliteiten voor preoperatieve en intra-operatieve beeldvormingsdoeleinden is dat men de kans loopt om ‘appels met peren’ te gaan vergelijken. Een mogelijke oplossing voor dit probleem zou kunnen liggen in het gebruik van (hybride) contrastmiddelen die zowel met een preoperatieve als een aanvullende intra-operatieve beeldvormingstechniek te identificeren zijn. Een klinisch voorbeeld hiervan is het hierboven beschreven ICG-99mTc-nanocolloid voor de schildwachtklierprocedure voor maligniteiten in het hoofd-halsgebied of prostaatkanker.8 9 Dit hybride contrastmiddel is in onze ogen slechts een eerste stap in de verdere contrastmiddelgebaseerde integratie van verschillende beeldvormingstechnieken, die kunnen bijdragen aan een betere ervaring voor zowel de patiënt als de arts.10
Thijs Engelen
onderzoeker Interventional Molecular Imaging Laboratorium (IMIlab), afdeling Radiologie LUMC, Leiden
Gijs KleinJan
onderzoeker IMIlab, afdeling Radiologie LUMC
Fijs van Leeuwen
hoofd IMIlab, afd. Radiologie LUMC, en onderzoeker afd. Hoofd-halschirurgie en Oncologie, NKI-AVL, Amsterdam
Nynke van den Berg
onderzoekster IMIlab, afd. Radiologie LUMC en onderzoekster afd. Urologie, NKI-AVL
Wij willen onze collega’s van de betrokken afdelingen van het NKI-AVL bedanken voor hun hulp en inzet, in het bijzonder Simon Horenblas, Henk van der Poel, Fons Balm en Martin Klop. Tevens bedanken wij onze collega’s van de afdeling Radiologie van het LUMC, in het bijzonder Arian van Erkel en Mark Burgmans en Daphne Rietbergen en Renato Valdés Olmos van de sectie Nucleaire Geneeskunde.
contact: n.s.van_den_berg@lumc.nl; cc: redactie@medischcontact.nl
Geen belangenverstrengeling gemeld
Het winnende filmpje Innovation for Health 2014:
Voetnoten
1. Older J. Anatomy: a must for teaching the next generation. Surgeon. 2004;2(2):79-90.
2. Okur A, Ahmadi SA, Bigdelou A, Wendler T, Nassir N. MR in OR: First analysis of AR/VR visualization in 100 intra-operative Freehand SPECT acquisitions, IEEE ISMAR 2011. DOI: 10.1109/ISMAR.2011.6092388.
3. Pinilla I, Rodriguez-Vigil B, Gomez-Leon N. Integrated FDG PET/CT: Utility and Applications in Clinical Oncology. Clin Med Oncol. 2008;2:181-198.
4. Mariani G, Bruselli L, Kuwert T, et al. A review on the clinical uses of SPECT/CT. Eur J Nucl Med Mol Imaging. 2010;37(10):1959-85.
5. Brouwer OR, van den Berg NS, Matheron HM, et al. Feasibility of intraoperative navigation to the sentinel node in the groin using preoperatively acquired SPECT/CT data; transferring functional imaging to the operating room. J Urol. 2014. DOI: 10.1014/j.juro.2014.03.127.
6. Brouwer OR, Buckle T, Bunschoten A, et al. Image navigation as a means to expand the boundaries of fluorescence-guided surgery. Phys Med Biol. 2012;57(10):3123-3136.
7. Engelen T, Winkel BMF, Rietbergen DDD, et al. The next evolution in radioguided surgery: Breast cancer related sentienl node localization using a freehandSPECT-mobile gamma camera combination”. Am J Nucl Med Mol Imaging. 2015. Accepted for publication.
8. van den Berg NS, Brouwer OR, Schaafsma BE, et al. Multimodal surgical guidance during sentinel node biopsy for melanoma: Combined gamma tracing and fluorescence imaging of the sentinel node through use of the hybrid tracer indocyanine green-technetium-99m-nanocolloid. Radiology. 2014. 17:140322. DOI: http://dx.doi.org/10.1148/radiol.14140322
9. KleinJan GH, van den Berg NS, Brouwer OR, et al. Optimisation of fluorescence guidance during robot-assisted laparoscopic sentinel node biopsy for prostate cancer. Eur Urol. 2014:66(6);991-8.
10. van den Berg NS, Valdes-Olmos RA, van der Poel HG, van Leeuwen FW. Sentinel lymph node biopsy for prostate cancer: a hybrid approach. J Nucl Med. 2013;54(4):493-6.

- Er zijn nog geen reacties














