Richtlijn is niet altijd heilig
Het behandelprotocol dat de richtlijn voorschrijft past niet bij elke patiënt
2 reacties
Uit drie recente casussen blijkt dat de richtlijn voor slokdarmkanker in de praktijk soms tekortschiet. Beredeneerd afwijken kan levens redden.
Huisarts Karen Konings constateerde in juni in Medisch Contact dat protocollen in de eerste lijn vaak niet aansluiten bij de behoefte van de individuele patiënt.1 Ook in de tweede en derde lijn loopt men hier tegenaan. Richtlijnen zijn een belangrijk onderdeel in de medische praktijk. Ze worden bij voorkeur toegepast; maar er kan van worden afgeweken, mits dit zorgvuldig in het dossier wordt vastgelegd. Het komt regelmatig voor dat de specifieke omstandigheden van een individuele patiënt niet in de beschikbare richtlijn zijn beschreven of dat verschillende alternatieve mogelijkheden worden aangegeven. In zo’n geval heeft het behandelteam ruimte om tot een gefundeerd eigen advies te komen. Maar onder welke omstandigheden mag men een advies geven dat expliciet indruist tegen zo’n richtlijn of een behandeling inhoudt waarvoor geen wetenschappelijke ondersteuning bestaat? In hoeverre is bijvoorbeeld de sterke behandelwens of jonge leeftijd van een patiënt hierbij een valide argument? Aan de hand van drie casussen willen wij enkele dilemma’s bespreken die zich kunnen voordoen bij de toepassing van richtlijnen.
Casus 1
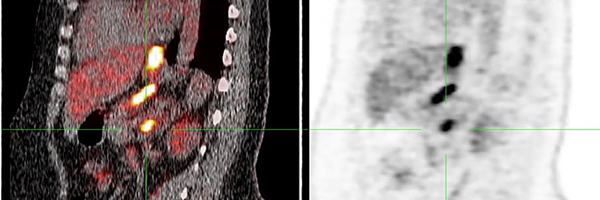
Een 34-jarige vrouw presenteerde zich met sinds kort bestaande passageklachten voor vast voedsel en 17 kg gewichtsverlies. Gastroscopie toonde distaal in de slokdarm een ulcus. In een biopt werd een adenocarcinoom vastgesteld. Een CT-scan toonde verdachte lymfeklieren boven in de buik. Hierop werd patiënte naar ons ziekenhuis doorverwezen.
Een PET/CT-scan toonde behalve de slokdarmtumor ook een vergrote lymfeklier nabij de arteria mesenterica superior (AMS) met verhoogde FDG-stapeling (FDG is een isotoop waarmee tumorweefsel kan worden opgespoord; zie figuur 1). Door de lokalisatie wordt deze klier als een afstandsmetastase (M1) beschouwd. Punctie leverde maligne cellen op, passend bij een metastase. Samenvattend werd de tumor klinisch gestadieerd als cT3N2M1-slokdarmcarcinoom.
In multidisciplinair overleg besloten we tot inductiechemotherapie buiten de geldende Nederlandse richtlijn.2 Evaluatie na de chemotherapie liet duidelijke afname van FDG-stapeling in de slokdarmtumor zien en thans volledig afwezige FGD-stapeling in alle lymfeklieren. Hierop werd besloten tot chirurgische exploratie.
Allereerst werd de lymfklier nabij de AMS uitgenomen; vriescoupe toonde geen restmaligniteit. Vervolgens werd een slokdarmresectie met lymfeklierdissectie en buismaagreconstructie uitgevoerd. Het postoperatieve beloop was ongecompliceerd. Het resectie-preparaat toonde een complete remissie (ypT0N0). Thans, drie jaar na operatie, is patiënte klinisch en radiologisch vrij van tumor en werkt zij weer voor 80 procent.
Casus 2
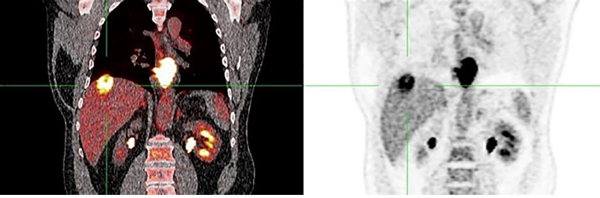
Een 59-jarige medicus presenteerde zich elders met thoracale pijnklachten bij omeprazolgebruik. Gastroscopie toonde een voor carcinoom verdachte laesie distaal in de slokdarm. Pathologisch onderzoek van een biopt toonde een matig gedifferentieerd plaveiselcelcarcinoom. Een CT-scan van thorax-abdomen liet enkele vergrote lymfeklieren zien. Tevens werd een leverhaard gediagnosticeerd verdacht voor metastase. Hierop werd patiënt naar ons doorverwezen.
PET/CT-scan liet de bekende leverhaard zien met intense FDG-stapeling (zie figuur 2) en enkele positieve lymfe-klieren, onder andere bij de truncus coeliacus. De slokdarmtumor werd klinisch gestadieerd als cT3N3M1-slokdarmcarcinoom.
Na multidisciplinair overleg hebben we conform de Nederlandse richtlijn geadviseerd om een punctie uit te voeren van de leverafwijking en bij pathologische bevestiging van de levermetastase te starten met palliatieve chemotherapie. Patiënt gaf echter aan in het buitenland een tweede mening te willen vragen gezien zijn uitgesproken wens tot chirurgie.
Nu, vier jaar later, vertelt patiënt dat hij zich indertijd tot een Belgisch ziekenhuis heeft gewend. Daar werd hij behandeld met chemotherapie gevolgd door een slokdarmresectie met synchrone leversegmentresectie. Het resectiepreparaat toonde een necrotische levermetastase en een radicaal verwijderde slokdarmtumor. Tot op heden is patiënt tumorvrij.
Casus 3
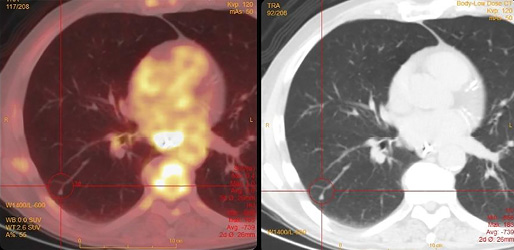
Een 65-jarige man presenteerde zich elders vanwege progressieve passageklachten. Bij gastroscopie werd een tumor gezien distaal in de slokdarm, dat een plaveiselcelcarcinoom bleek te betreffen. Op een gecombineerde PET/CT-scan werden naast de slokdarmtumor twee nodulaire laesies in de rechterlong waargenomen met matige FDG-opname (zie figuur 3). Gezien de sterke verdenking op longmetastasen werd gekozen voor palliatieve uitwendige radiotherapie (39Gy) op de primaire tumor. Hierop verbeterden zijn passageklachten.
Drie maanden later werd een nieuwe CT-scan vervaardigd. De niet-bestraalde nodulaire laesies in de rechterlong waren volstrekt onveranderd van grootte. Wederom werd besloten tot palliatie. Patiënt kwam vervolgens naar ons ziekenhuis voor een second opinion.
Zijn dysfagieklachten waren weer fors toegenomen zodat werd gestart met sondevoeding. Na uitvoerig overleg werd mede gezien de gunstige reactie op radiotherapie besloten tot een in opzet curatieve operatieve behandeling. De maligne aard van de beide onbehandelde longafwijkingen werd onvoldoende bewezen geacht, zeker nu deze gedurende een halfjaar stabiel in grootte waren gebleven.
Er werd gestart met resectie van een van beide longafwijkingen. Peroperatief vriescoupeonderzoek toonde het beeld van een benigne intrapulmonale lymfe-klier. Tijdens dezelfde operatie werd vervolgens een slokdarmresectie met buismaagreconstructie uitgevoerd. Het resectiepreparaat toonde een ypT3N1- plaveiselcelcarcinoom. Het postoperatieve beloop werd gecompliceerd door een naadlekkage van de oesofago-gastrostomie met een secundair thoraxempyeem waarvoor heroperatie nodig was. Tot op heden, nog slechts twaalf maanden na de operatie, is patiënt klinisch vrij van tumorrecidief.
Ethisch dilemma
Richtlijnen fungeren als leidraad bij de behandeling van veel ziektebeelden, waaronder slokdarmkanker. Patiënten worden meestal volgens de wetenschappelijk onderbouwde richtlijnen behandeld. Er zijn echter situaties waarin van een richtlijn kan worden afgeweken. Hierbij wordt het behandelteam soms voor een ethisch dilemma geplaatst tussen enerzijds de maximale behandelwens van de patiënt en anderzijds het do not harm-principe.
De huidige richtlijn voor het slokdarmcarcinoom is helder en eenduidig: in aanwezigheid van een lymfekliermetastase buiten het operatiegebied (zoals in casus 1) of een hematogene metastase (casus 2) is slechts plaats voor palliatieve behandeling. Op goede gronden kan men echter van de richtlijn afwijken. De argumenten voor zo’n besluit moeten in het dossier helder worden vastgelegd. Verschillende argumenten kunnen een rol spelen. Allereerst de leeftijd en conditie van patiënt. Zo is men bij een jonge patiënt met blanco voorgeschiedenis (casus 1) eerder bereid voor een ‘agressieve’ behandeling buiten de richtlijn te kiezen. Daarnaast spelen de mogelijke risico’s van een extraprotocollaire behandeling een rol. Een slokdarmresectie kan gepaard gaan met substantiële postoperatieve morbiditeit en zelfs mortaliteit, hetgeen moet worden afgewogen tegen de kans op genezing.3 Uit de colorectale metastasechirurgie is bekend dat de kans op succes mede afhangt van aantal, grootte en plaats van de levermetastasen. Indien voor inductiechemotherapie wordt gekozen, zal van een substantiële respons sprake moeten zijn (casus 1), alvorens te besluiten tot operatie.
Een bijzondere situatie doet zich voor als van een vermeende afstandsmetastase niet (eenvoudig) een betrouwbaar biopt kan worden verkregen, zoals bij de patiënt in casus 3. Afhankelijk van de genoemde factoren zal men dan minder of juist meer geneigd zijn de patiënt het voordeel van de twijfel te geven. Door de grootte van de (vermeende) metastase te vervolgen tijdens chemo(radio)therapie kan indirect meer zekerheid worden verkregen over de aard van de laesie.
Geringe aantallen
Volgens de Wet medisch-wetenschappelijk onderzoek met mensen (WMO) is het bij een experimentele behandeling verplicht dat een door een medisch-ethische commissie goedgekeurd onderzoeks-protocol voorhanden is, dat de patiënt na voorlichting schriftelijk toestemming heeft verleend en dat de onderzoeksresultaten worden gerapporteerd. Hoewel niet wettelijk verankerd, zou hetzelfde moeten gelden voor een behandeling buiten de bestaande richtlijn. Juist dan is transparantie en kritische intercollegiale toetsing voorafgaande aan uitzonderlijke behandeling extra belangrijk. Het multidisciplinaire (oncologische) overleg dat tegenwoordig in vrijwel alle ziekenhuizen functioneert, is daarvoor een geschikt gremium. Omdat het per definitie gaat om uitzonderingsgevallen, zijn de aantallen te gering om per ziekenhuis iets zinvols te kunnen zeggen over het nut van de toegepaste therapie. Waar mogelijk verdient het daarom aanbeveling de patiënt te includeren in een (inter)nationaal register, opdat ook achteraf toetsing kan plaatsvinden en uit dergelijke behandelingen lering kan worden getrokken.
Als stelregel heeft een patiënt uiteraard altijd het recht om een medisch geïndiceerd geachte behandeling te weigeren. Het omgekeerde is veel ingewikkelder.4 Slechts in uitzonderlijke gevallen kan een patiënt een behandeling afdwingen waarvoor op medische gronden strikt genomen geen indicatie bestaat. De patiënt in casus 2 had slokdarmkanker met een levermetastase en was door zijn eigen medische achtergrond goed in staat mee te denken over het behandelplan. Hij gaf herhaaldelijk aan tot het uiterste te willen gaan en een sterke voorkeur te hebben voor een operatie. Zijn belangrijkste argument was dat de kwaliteit van zijn leven niet zozeer door zijn fysieke ongemakken werd bepaald, maar door de wetenschap ‘opgegeven’ te zijn als patiënt. Hij voelde zich hierin onvoldoende gehoord. Vooral het feit dat niet zijn wens maar het oordeel van het behandelteam bepalend zou zijn geweest, leidde tot zijn keuze voor een behandeling in het buitenland. Daar worden regelmatig behandelindicaties gesteld die door de Nederlandse beroepsgroep niet worden onderschreven. Mede onder druk van negatieve berichten in de lekenpers kan het dan verleidelijk zijn – maar zeker niet altijd verstandig – om als behandelend arts de ruimere indicatiestelling over te nemen.5
Voor patiënten met slokdarmkanker en een geïsoleerde levermetastase hebben wij onlangs voorgesteld een landelijk register op te zetten. Deze patiënten willen wij na strikte selectie een behandeling aanbieden bestaande uit inductiechemotherapie, resectie van de levermetastase, neoadjuvante chemoradiotherapie en uiteindelijk slokdarmresectie.
Onderlinge toetsing
Wij concluderen dat onder bijzondere omstandigheden van een richtlijn kan worden afgeweken, mits de argumentatie hiervoor zorgvuldig wordt vastgelegd. De wens van een individuele patiënt tot agressieve behandeling is slechts een van de factoren die hierbij een rol spelen. Het verdient aanbeveling om extraprotocollaire behandelingen centraal te registeren om onderlinge toetsing mogelijk te maken en uiteindelijk daaruit lering te kunnen trekken.
dr. Jan Willem van den Berg, aios chirurgie, Erasmus MC, Rotterdam
dr. Bas Wijnhoven, chirurg, Erasmus MC, Rotterdam
dr. Ate van der Gaast, internist-oncoloog, Erasmus MC, Rotterdam
prof. dr. Jan van Lanschot, chirurg, Erasmus MC, Rotterdam
contact
cc: redactie@medischcontact.nl
Geen belangenverstrengeling gemeld door de auteurs.
Lees ook:
Referenties
1. Konings K. Patiënt past niet in protocol; nuttig voor de organisatie van zorg, maar niet voor de individuele patiënt. Medisch Contact. 2016; 24: 36-9.
2. IKNL. Oesofaguscarcinoom, Landelijke richtlijn, Versie: 3.1.2015. (http://www.oncoline.nl/oesofaguscarcinoom)
3. Jaarrapportage Dutch Upper GI Cancer Audit (DUCA). 2014. (https://www.dica.nl/jaarrapportage-2014/duca.html)
4. Schoemaker CG, van der Weijden T. Patiëntvoorkeur versus evidencebased medicine; hadden de pioniers van EBM oog voor wat de patiënt wil? Ned Tijdschr Geneeskd 2016; 160 (24): 39-42.
5. de Vreede J. In Nederland opgegeven, in België wel behandeld. http://www.ad.nl/ad/nl/4560/Gezond/article/detail/3638307/2014/04/19/In-Nederland-opgegeven-in-Belgie-genezen-van-kanker.dhtml. Algemeen Dagblad. 19-04-2014.
pdf















Wim van der Pol
oud ziekenhuisapotheker, Delft
De klinische les doet mij sterk denken aan de situatie van de tijd dat er nog geen richtlijnen bestonden. Chirurgen overlegden met elkaar en vaak voerde de chirurg met de meeste ervaring (en soms heroïek) de operatie uit. Nu zijn er richtlijnen, die ...eigenlijk hulplijnen genoemd zouden kunnen worden. Dat betekent dat niet alles in richtlijnen gevat dient te worden; met de argumenten die in de klinische les genoemd worden: registratie, experimenteel, onderzoek, opleiding etc. En zo zijn er nog meer varieteiten te benoemen.
Derk Arts
Arts-onderzoeker, Amsterdam
Een mooie beschouwing, dank. Een vergelijkbare conclusie trokken wij in deze paper:
http://www.ijmijournal.com/article/S1386-5056(16)30029-6/abstract
Onze conclusie was dat de meeste voorkomende redenen voor non-adherentie vielen onder contra-indica...ties (die niet expliciet in de richtlijn werden benoemd) en patient voorkeuren (zoals ook uit uw beschouwing blijkt).