Biotechnologie gaat praktijk veranderen
Plaats een reactieHet zal niet lang meer duren of sleutelen aan de genen behoort tot het vaste arsenaal van de dokter, aldus een trendanalyse van onder meer de Gezondheidsraad. Om welke technieken gaat het, en wat zijn de gevolgen?
Ze zullen grote impact hebben op de geneeskundige praktijk – de biotechnologische ontwikkelingen die de COGEM (Commissie Genetische Modificatie) en de Gezondheidsraad, ondersteund door de WRR, inventariseren in de Trendanalyse biotechnologie. Kort samengevat komen de nieuwe biomedische technieken neer op: genen in kaart brengen, genetisch sleutelen en synthetische biologie, zoals het maken van kunstmatige organen en weefsels (zie kaders).
Genen in kaart
Next generation sequencing (NGS) maakt het mogelijk veel genen tegelijk in kaart te brengen. Dat kan een set genen zijn waarvan bekend is dat ze met een specifieke groep aandoeningen geassocieerd zijn (een ‘panel’), maar je kunt ook het gehele genoom in beeld krijgen (whole genome sequencing). Dat laatste zal in Nederland breed worden toegepast, zo is de verwachting.
NGS is ook zeer geschikt voor screening, zoals het niet-invasief prenataal testen (NIPT). Denk ook aan preconceptie-dragerschapstesten voor paren met een kinderwens; een aantal umc’s biedt deze testen voor meerdere ziekten tegelijk al aan. In de oncologie wordt NGS gebruikt om het DNA van de tumorcellen van de patiënt te sequensen om zo te kunnen beoordelen welke therapie de meeste kans van slagen heeft; een voorbeeld van personalized medicine (waarover volgende week meer in een special van Medisch Contact).
‘De ontwikkelingen gaan razendsnel’, constateert Pim van Gool, voorzitter van de Gezondheidsraad en hoogleraar neurologie aan het AMC. ‘Toen dit dossier zich aandiende heb ik onze oude trendanalyses er nog even bij gepakt. Als je die oudere rapporten leest, snap je dat menigeen dacht: “Eerst maar eens zien wat het allemaal wordt”. Die speelruimte hebben we nu niet meer. De reikwijdte van de nieuwe technieken is groter en de urgentie om na te denken over de gevolgen is veel hoger. Bedoeling van de trendanalyse is dan ook om al deze ontwikkelingen op het netvlies te brengen, van de samenleving en de politiek.’
Het rapport bepleit ‘flexibel inspelen op nieuwe ontwikkelingen zoals NGS en CRISPR-Cas’. Guido de Wert, hoogleraar biomedische ethiek (Universiteit Maastricht), is het daarmee eens. ‘Doe empirisch-ethisch onderzoek. Verken in de praktijk of clinici met regels en richtlijnen uit de voeten kunnen en of de belangen en rechten van patiënten voldoende beschermd zijn.’
Hij geeft een voorbeeld: ‘De nieuwe sequencingtechnieken hebben vanwege de breedte en complexiteit ervan consequenties voor de vereiste informed consent. We moeten af van de traditionele invulling waarbij de patiënt over iedere mogelijke uitslag van een test in principe vooraf al in detail moet zijn geïnformeerd om vervolgens op basis daarvan toestemming te geven. We zullen op zoek moeten naar aangepaste vormen. Hoe kan worden gewaarborgd dat ook meer algemene en gefaseerde informatie valide toestemming mogelijk maakt?’
Zo zijn er meer kwesties, memoreert Van Gool. ‘Hoe om te gaan met nevenbevindingen die next generation sequencing ongetwijfeld zal opleveren? En wat is de waarde van voorspellende genetische diagnostiek? Er wordt weliswaar flink getamboereerd op personalized medicine, maar uitspraken over de verwachte werking van medicamenten zullen altijd een onzekerheidsmarge houden. Stel dat ik op basis van iemands genetische opmaak vaststel dat een ‘last resort-geneesmiddel’ bij hem hoogstwaarschijnlijk niet zal werken, en stel dat deze patiënt radeloos is, dan moet ik daarover als dokter wel heel zeker zijn. Misschien dat ik dan toch maar kies voor een proefbehandeling.’
Genetisch sleutelen
Sleutelen aan de genen zal, verwacht het trendrapport, ‘een vaste waarde’ worden in de geneeskunde. Er zijn – of komen – in hoofdlijnen drie technieken beschikbaar. Met CRISPR-Cas is het mogelijk om de expressie van genen te reguleren, gericht kleine veranderingen (puntmutaties) aan te brengen, (delen van) genen te verwijderen, of nieuwe genen of DNA-fragmenten op specifieke plekken in het erfelijke materiaal te introduceren. Er zijn twee toepassingen bij de mens mogelijk: ziekmakende genen of mutaties verwijderen of veranderen in lichaamscellen, een variant van gentherapie. Deze ingrepen zijn er nog niet. De andere zou kiemcelmodificatie zijn; momenteel verboden in de EU.
RNA interference (RNAi) maakt het mogelijk om de expressie van genen te blokkeren zonder het DNA te veranderen. Als zo de volgorde van het genoom niet wordt gewijzigd gaat het strikt genomen overigens niet om genetische modificatie.
En dan is er gentherapie, waarbij DNA of RNA in lichaamscellen wordt gebracht om een ziekte te behandelen. Om het erfelijke materiaal op de plaats van bestemming te krijgen wordt een ‘vector’ gebruikt: vaak een onschadelijk gemaakt virus, maar ook nanodeeltjes zijn inmiddels in beeld. Veelbelovende resultaten zijn experimenteel geboekt bij de behandeling van B-celleukemie en hemofilie B en bij kankerpatiënten bij wie T-cellen genetisch zijn gemodificeerd zodat ze tumorcellen herkennen en aanvallen.
Debat
Ook sleutelen aan de genen is niet zonder problemen. ‘CRISPR-Cas is een doorbraak en bredere implementatie zal niet lang op zich laten wachten’, verwacht De Wert. ‘De hete aardappel is ongetwijfeld gene-editing in de menselijke kiembaan. De te voeren discussie zal grotendeels een kloon zijn van het debat zo’n dertig jaar geleden over kiembaangentherapie. Maar dat was toen een theoretisch debat, omdat de beschikbare technieken tekortschoten. Dat geldt niet voor CRISPR-Cas.’
Mogelijk komt daarmee ook het debat over human enhancement op de agenda: het introduceren van gewenste eigenschappen in het menselijk genoom. De Wert: ‘Sommige experts vinden dat een non-issue. Eigenschappen als intelligentie of muzikaliteit zijn genetisch veel te complex en sterk afhankelijk van omgeving – enhancement is sciencefiction, zeggen zij. Misschien is dit te kort door de bocht. Sommige “verbeteringen” zijn moleculair mogelijk eenvoudiger te realiseren dan zij denken, denk bijvoorbeeld aan een genetisch verhoogde weerstand tegen infectieziekten.’
Nieuwe weefsels
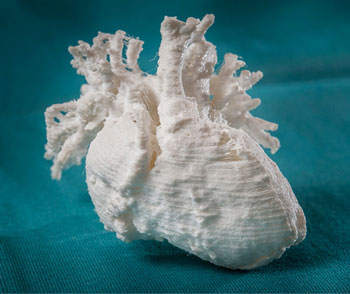
Met behulp van 3D bioprinten is het mogelijk om zachte weefsels en botweefsel voor reconstructieve ingrepen te maken. Deze prints verkeren nu nog in een experimenteel stadium, en worden gebruikt voor het maken van ziektemodellen en het testen van geneesmiddelen. Ook kunnen op deze manier organoids worden gemaakt; miniatuur-organen die functies van hersen-, hart-, lever of darm-cellen kunnen nabootsen.
Van Gool en De Wert zijn het erover eens dat de bestaande regelgeving te exclusief is gericht op veiligheid. Van Gool: ‘Het is goed om steeds de veiligheid af te wegen tegen de potentiële winst van een nieuwe techniek. Zoals we in de dagelijkse klinische praktijk ook gunstige werkingen van behandelingen altijd afwegen tegen bijwerkingen.’
Henk Maassen
Webverwijzing:
De trendanalyse Biotechnologie 2016
Lees ook:

- Er zijn nog geen reacties



















